Las fuerzas que mantienen unidos a los átomos tienen naturaleza electroestática, es decir, fuerzas atractivas entre cargas de distinto signo.
Características de cada tipo de enlace:
Enlace covalente:
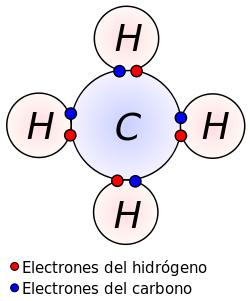
Es el enlace que utilizan los átomos de elementos químicos no metálicos al unirse. La configuración de gas noble se alcanza por compartición de electrones de la capa de valencia de dichos átomos.
El enlace covalente está basado en la compartición de electrones de la capa de valencia. Los electrones compartidos atraen a los núcleos de los átomos, quedando estos últimos unidos entre sí.
Enlace iónico:
Se llama también electrovalente, y tiene lugar cuando se unen átomos de elementos metálicos con átomos de elementos no metálicos. En él, los átomos alcanzan la configuración de gas noble por transferencia de los electrones de la capa de valencia del metal a la capa de valencia del no metal.
El enlace iónico se basa en la transferencia de electrones entre dos átomos, lo que conlleva la formación de iones positivos e iones negativos que se atraen mediante fuerzas de tipo electrostático.
Enlace metálico:
Es característico de los metales. En este tipo de enlace también se comparten electrones, pero de una forma algo diferente.
El enlace metálico está basado en la cesión de los electrones de la capa de valencia de cada uno de los átomos de metal. Se forma así una nube electrónica que envuelve y atrae a los iones positivos metálicos.
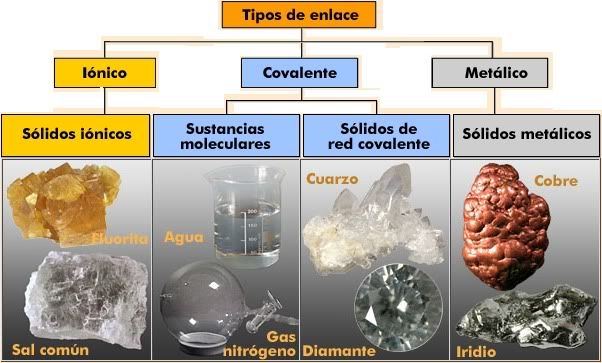
Esquema resumen


Grand Bay Resort & Casino - MapYRO
ResponderEliminarCasino in 구미 출장샵 Bay, California. 1010 South Shore Drive. Hayward, CA 95464. Directions · (800) 383-8000. Call Now · More 오산 출장샵 Info. Hours, Accepts Credit Cards, 경산 출장샵 Wi-Fi, PokéStop 대전광역 출장안마 Rating: 2 · 1 vote · Price range: 김제 출장안마 $